Črevná mikrobiota a metabolizmus sacharidov v normálnom stave a pri patológii
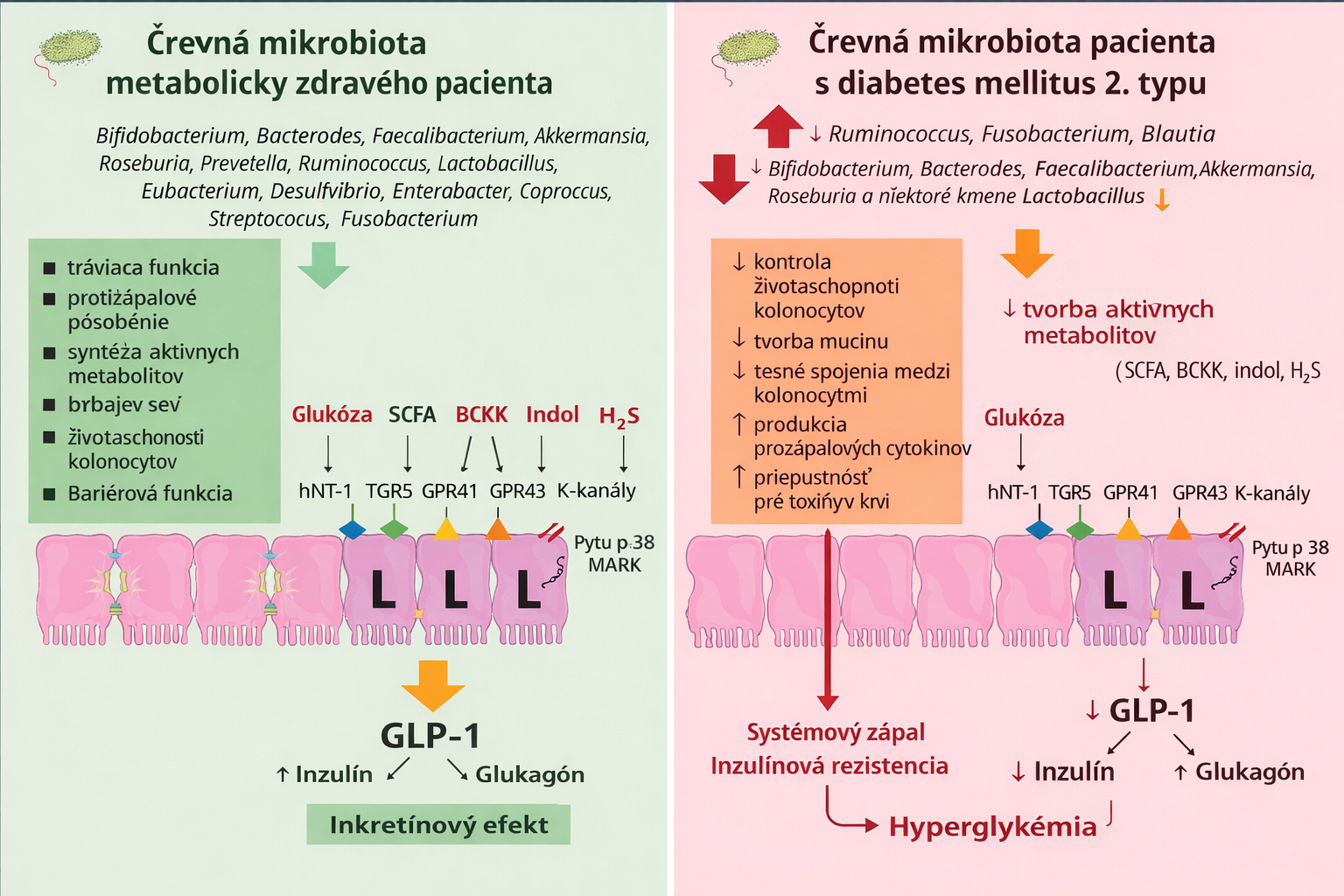
Črevná mikrobiota môže byť považovaná za samostatný orgán, ktorý plní rôzne funkcie vrátane vplyvu na syntézu a uvoľňovanie viacerých hormónov, ako sú GLP-1, GIP, peptid tyrozín-tyrozín (PYY), serotonín, cholecystokinín, inzulín a ďalšie. Súvislosť medzi inkretínovými hormónmi, inzulínom a mikrobiótou zohráva významnú úlohu v patofyziológii aj v možnej korekcii metabolických porúch.
Krátkoreťazové mastné kyseliny (SCFA), ktoré vznikajú pri sacharolytickom kvasení nestrávených sacharidov v črevnej mikrobióte, ovplyvňujú črevnú glukoneogenézu, metabolizmus sacharidov a tukov aj syntézu inkretínov a inzulínu. Receptory pre SCFA (GPR41 a GPR43) sa nachádzajú na povrchu enteroendokrinných buniek čreva (L- a K-buniek), v pečeni, bielom tukovom tkanive, kostrových svaloch a na β- a α-bunkách pankreasu.
Aj ďalšie mikrobiálne metabolity ovplyvňujú inkretínové hormóny. Sírovodík môže podporovať syntézu GLP-1 pôsobením na L-bunky. Receptorové mechanizmy tohto pôsobenia však zatiaľ nie sú známe. Indol slúži ako signálna molekula pre L-bunky a preukázateľne reguluje sekréciu GLP-1. Sekundárne žlčové kyseliny (dezoxycholová a litocholová) tiež môžu ovplyvňovať tvorbu GLP-1.
U pacientov s metabolickými poruchami, akými sú obezita a cukrovka 2. typu (DM2), sa často pozorujú výrazné zmeny v zložení črevnej mikrobioty: znížená alfa-diverzita, nerovnováha v zastúpení jednotlivých rodov a druhov baktérií a následne znížená tvorba SCFA, indolu, sírovodíka a sekundárnych žlčových kyselín. To negatívne vplýva na reguláciu syntézy a sekrécie inkretínových hormónov.
Najaktívnejšie pri tvorbe uvedených metabolitov sú baktérie rodov Bifidobacterium, Bacteroides, Faecalibacterium, Akkermansia, Roseburia, Prevotella, Ruminococus, Lactobacillus, Clostridium, Eubacterium, Desulfovibrio, Enterobacter, Coprococcus, Eubacterium, Streptococcus, Fusobacterium. Viaceré štúdie potvrdzujú, že práve tieto rody sa pri obezite a DM2 významne znižujú. Okrem tvorby prospešných metabolitov sa podieľajú aj na udržiavaní nepriepustnosti črevnej bariéry, syntéze protizápalových cytokínov a podpore diferenciácie a rastu epitelových buniek. Vďaka týmto mechanizmom znižujú riziko vzniku systémového zápalu, ktorý je spúšťačom porúch metabolizmu sacharidov.
U pacientov s DM2 sa často zaznamenáva zvýšené zastúpenie Fusobacterium nucleatum a Ruminococcus gnavus, ktoré vedie k prudkému nárastu produkcie prozápalových cytokínov (IL-1, IL-6, TNF-α). Zároveň dochádza k narušeniu priepustnosti črevnej bariéry. Kombinácia týchto faktorov spôsobuje, že IL-1, IL-6, TNF-α a lipopolysacharidy (LPS) prechádzajú do krvného obehu a vedú k rozvoju chronického nízkostupňového systémového zápalu.
Možno predpokladať, že prozápalový stav vznikajúci pri nerovnováhe medzi prozápalovými a protizápalovými cytokínmi, ako aj zníženie ochranného pôsobenia SCFA na epitelové bunky, prispievajú k šíreniu zápalu aj na L- a K-bunky čreva. To môže viesť k ich dysfunkcii a k zníženiu produkcie a sekrécie GLP-1 a GIP.
U pacientov s poruchami metabolizmu sacharidov sa teda pozorujú zmeny v štruktúre črevnej mikrobioty aj zníženie koncentrácie inkretínových hormónov v krvi. Tieto zmeny, spolu s ďalšími patogenetickými faktormi (chronický zápal, inzulínová rezistencia, dysfunkcia β-buniek pankreasu a pod.), prispievajú k rozvoju cukrovky 2. typu (pozri Obrázok 1).
Obrázok 1. Porovnanie vplyvu črevnej mikrobioty na metabolizmus sacharidov u metabolicky zdravého človeka a pacienta s cukrovkou 2. typu [1].
Vplyv liečby analógmi GLP-1 na črevnú mikrobiotu
V rade predklinických aj klinických štúdií sa skúmal vplyv analógov GLP-1 na črevnú mikrobiotu (pozri Tabuľku 1).
Tabuľka 1. Modulácia črevnej mikrobioty v štúdiách na zvieratách a u pacientov s cukrovkou 2. typu na pozadí použitia analógov GLP-1 [2-10].
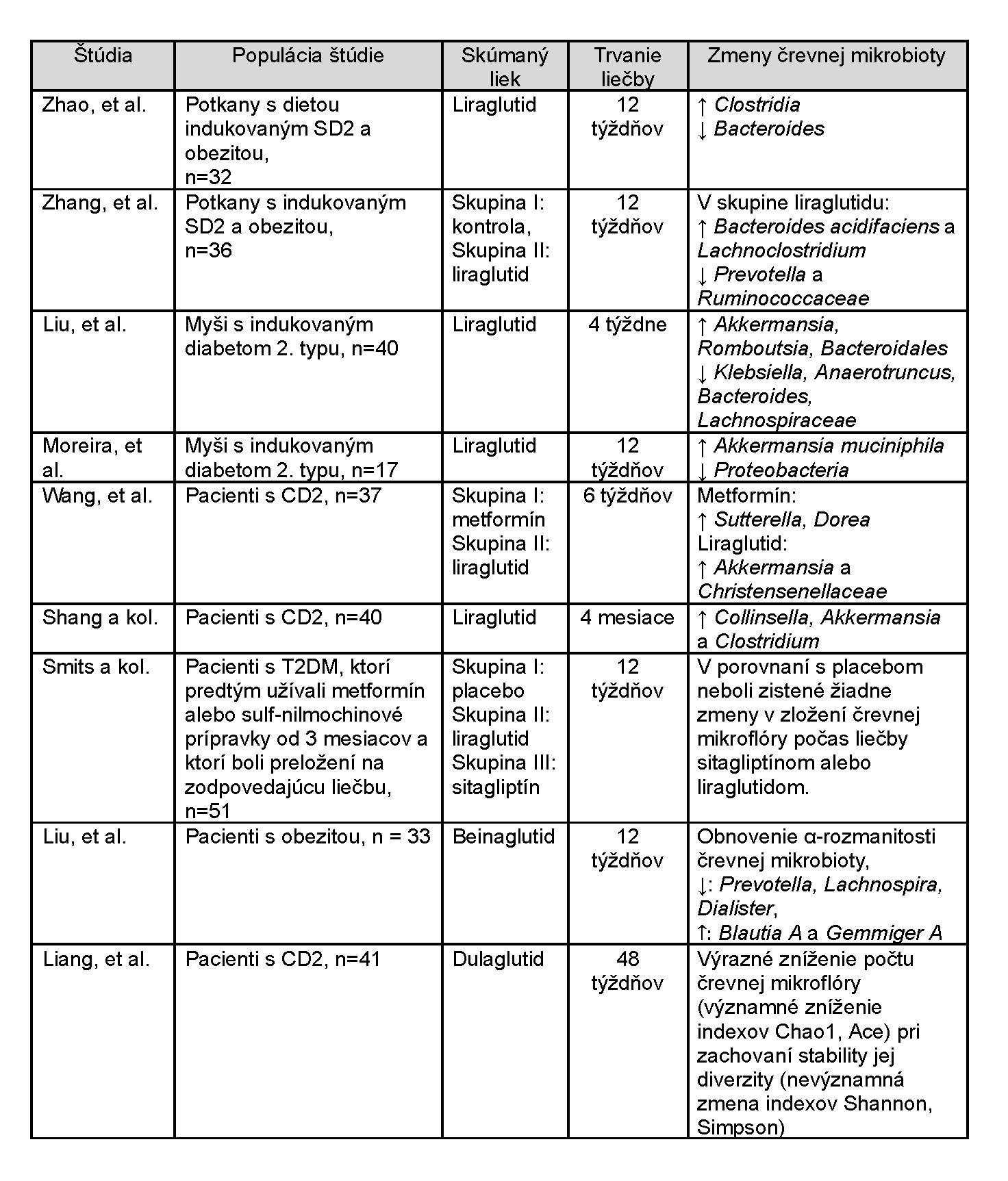
Počet štúdií, ktoré hodnotia modifikáciu črevnej mikrobioty na pozadí liečby liekmi inkretínovej rady, je v súčasnosti obmedzený. Vo väčšine prípadov ide o štúdie na laboratórnych zvieratách alebo klinické štúdie s malým počtom pacientov, čo sťažuje posúdenie zákonitostí zmien zloženia mikrobioty počas liečby. Získané údaje podnecujú k ďalším štúdiám zameraným nielen na hodnotenie charakteru zmien črevnej mikrobioty, ale aj na skúmanie jej účinnosti a bezpečnosti v závislosti od počiatočného zloženia mikrobioty. Tieto výsledky môžu umožniť určiť individuálny prístup k pacientom s poruchami metabolizmu uhľohydrátov a vyvinúť prediktívne modely účinnosti a bezpečnosti vykonávanej terapie.