Čo je to rezolúcia zápalu a čím sa farmakologické potlačenie zápalu líši od jeho prirodzenej rezolúcie
Zápal je prirodzená obranná reakcia organizmu na poškodenie jeho tkanív a buniek, preniknutie patogénnych mikroorganizmov alebo pôsobenie dráždivých látok, ktorá pomáha odstrániť poškodenie a obnoviť celistvosť poškodených tkanív. Medzi hlavné príznaky zápalu, opísané už v 1. – 2. storočí významnými starorímskymi lekármi Celsom a Galenom, patria: teplo (calor), sčervenanie (rubor), opuch (tumor), bolesť (dolor) a porucha funkcie (functio laesa) orgánu alebo časti tela (pozri obr. 1, červená farba).
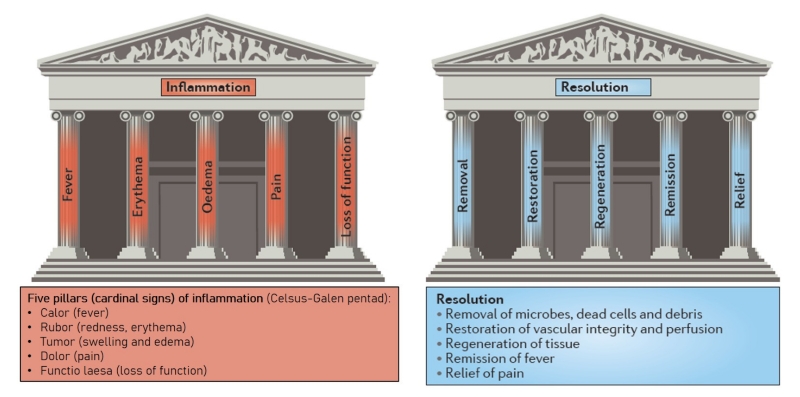
Je jasné, prečo vzniká zápal, ale ako a prečo ustupuje alebo „rezolúcia“? Súčasné výskumy, napríklad tie, ktoré vykonal profesor Charles N. Serhan a jeho kolegovia z Harvard Medical School, umožňujú vnímať rezolúciu zápalu ako aktívny proces a opisujú molekulárne a bunkové procesy, ktoré sa pri tom odohrávajú. Podobne ako príznaky zápalu, možno ich nazvať „hlavnými príznakmi vyriešenia“, a to: odstránenie mikroorganizmov, dráždivých látok, mŕtvych a poškodených buniek; obnovenie integrity ciev a krvného obehu; regenerácia tkanív, odstránenie horúčky a zmiernenie zápalovej bolesti (pozri obr. 1, modrá farba).
Resolúcia zápalu je dôležitou a záverečnou fázou – ide o aktívny proces, ktorý umožňuje návrat k homeostáze. Ak sa zápalová reakcia včas „nevypne“, môže dôjsť k nadmernému alebo chronickému zápalu.
Imunitný systém zastavuje zápalovú reakciu pomocou špecializovaných mediátorov riešenia zápalu (Specialized Pro-Resolving Mediators, SPM). SPM pôsobia ako stop signály zápalovej reakcie. Pomáhajú „vyčistiť“ poškodenú oblasť od bunkového odpadu, posilňujú regeneráciu tkanív a zmierňujú bolesť. SPM sa v našom organizme syntetizujú z omega-3 (EPA a DHA) a sú molekulami, ktoré vykazujú aktivitu prispievajúcu k riešeniu zápalu.
Existuje množstvo farmakologických prípravkov schopných bojovať so zápalom. Zvyčajne potláčajú aktívnu zápalovú reakciu tým, že blokujú nejakú dôležitú fázu jej patogenézy. Medzi takéto prípravky patria:
· Nesteroidné protizápalové lieky (NPL), napríklad kyselina acetylsalicylová, diklofenak, ibuprofén, ketoprofen, meloxikam, celekoxib a iné, inhibujú aktivitu enzýmov cyklooxygenáz (COX-1/COX-2), čo vedie k zníženiu syntézy mediátorov zápalu (prostaglandínov a tromboxanu).
· Glukokortikosteroidy (GKS), napríklad prednizolón, dexametazón, betametazón, budezonid, flutikazón, ktoré sa viažu na cytoplazmatické glukokortikoidné receptory, čo vedie k potlačeniu transkripcie mnohých prozápalových génov zodpovedných za produkciu cytokínov, enzýmov, adhezínov a iných látok.
· Bazálne protizápalové lieky (BPL) používané pri reumatoidnej artritíde a iných autoimunitných ochoreniach, napríklad metotrexát, leflunomid, sulfasalazín, hydroxychlorochín, azatioprín, modulujú proliferáciu lymfocytov, syntézu cytokínov a autoantitiel; spomaľujú progresiu zápalového poškodenia kĺbov.
· Biologické lieky (monoklonálne protilátky), napríklad infliksimab, adalimumab, tocilizumab, rituximab, anatelizumab, ixolizumab, blokujú určité cytokíny (TNF-α, IL-1, IL-6, IL-17, IL-23) alebo ich bunkové receptory, čo vedie k výraznému potlačeniu zápalu.
Existujú aj iné lieky s protizápalovým účinkom, avšak všetky potláčajú zápal – znižujú tvorbu mediátorov zápalu a intenzitu jeho príznakov, ale v pravom zmysle slova zápal neodstraňujú. Môžu byť veľmi účinné pri kontrole symptómov tým, že blokujú zápalovú reakciu, ale pritom neodstraňujú poškodenie tkanív, nepodporujú odstraňovanie odumretých buniek a spravidla pritom potláčajú imunitu. V konečnom dôsledku to môže ovplyvniť schopnosť organizmu bojovať s infekciami a inými ochoreniami.
SPM naopak nepotláčajú imunitný systém na účely odstránenia zápalu, ale odstraňujú (ukončujú) ho prirodzenou cestou. To neznamená, že SPM majú protizápalové účinky porovnateľné so silou a trvaním vyššie uvedených liekov a že by ich mohli nahradiť – takéto údaje nemáme k dispozícii. Produkty obsahujúce SPM alebo zvyšujúce produkciu SPM, ktoré dopĺňajú základnú liečbu a smerujú k vyriešeniu zápalu prirodzenejšou cestou, možno však považovať za perspektívny smer pre budúci výskum a vývoj. Na to nepriamo poukazujú už vykonané štúdie, ktoré preukázali zníženú hladinu SPM v tkanivách u pacientov s rôznymi ochoreniami (pozri ďalej).
Čo ukázali štúdie špecializovaných mediátorov riešenia zápalu (SPM) a prečo sú klinické výsledky použitia omega-3 pri rôznych ochoreniach často protichodné
Nekontrolovaný zápal zohráva dôležitú úlohu pri mnohých chronických ochoreniach, vrátane artritídy, kardiovaskulárnych ochorení, rakoviny, autoimunitných ochorení, infekcií, niektorých neurodegeneratívnych ochorení (Alzheimerova choroba) a ďalších.
Nesprávne načasované a neúplné vyliečenie zápalu významne ovplyvňuje zdravotný stav pacienta, kvalitu jeho života a podstatne spomaľuje úplné uzdravenie. Výskumy ukazujú, že v porovnaní so zdravými ľuďmi majú pacienti s mnohými chronickými zápalovými ochoreniami v krvi a postihnutých tkanivách výrazne zníženú hladinu SPM.
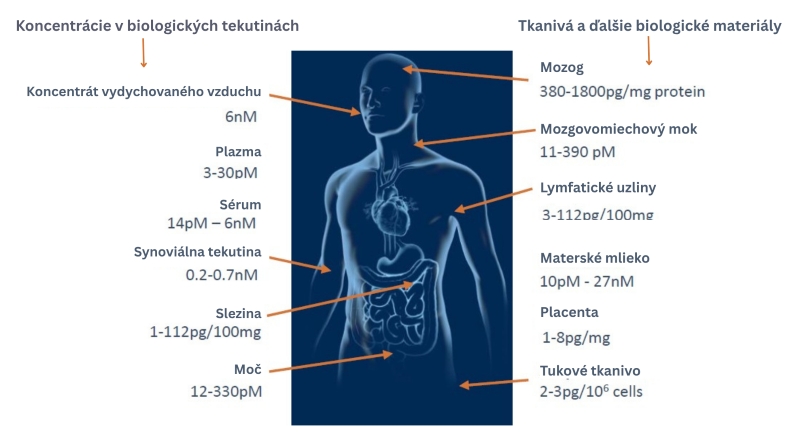
SPM boli zistené v rôznych tkanivách a orgánoch človeka v širokom rozmedzí nízkych, ale biologicky aktívnych hladín, ktoré sa očakávane zvyšujú v prípade vzniku zápalovej reakcie a jej prechodu do fázy liečby (pozri obr. 2).
Nie vždy je to však tak a u niektorých pacientov sa pri viacerých ochoreniach, ako sú:
· artritída,
· kardiovaskulárne ochorenia,
· obezita,
· cukrovka 2. typu,
· metabolický syndróm,
· bronchiálna astma,
· zápalové ochorenia čriev (ulcerózna kolitída, Crohnova choroba),
· mukoviscidóza,
· endometrióza,
· mastitída,
· Alzheimerova choroba,
· systémový lupus erythematosus,
· po chirurgických zákrokoch,
· pri rade ďalších patologických stavov.
Jednou z možných príčin nízkych hladín SPM u týchto pacientov je to, že mechanizmy, ktoré premieňajú omega-3 na SPM, nemusia fungovať správne. To má priamy vplyv aj na možné účinky omega-3, ktoré sa dostávajú do organizmu s potravou a dodatočne sa užívajú vo forme doplnkov stravy alebo liekov
Mnohé prospešné účinky omega-3 mastných kyselín na zdravie sú dobre známe a všeobecne uznávané nielen vedeckými organizáciami, ale aj regulačnými orgánmi v rôznych krajinách, a to za predpokladu ich dostatočného príjmu do organizmu: podpora normálneho vývoja očí a mozgu u plodu a dojčených detí a normálneho vývoja zraku u detí do 12 mesiacov; podpora normálnej činnosti srdca, normálnej hladiny cholesterolu a triglyceridov v krvi, normálneho krvného tlaku, normálnej funkcie mozgu a normálneho zraku u dospelých. O týchto účinkoch môžu legálne informovať výrobcovia doplnkov stravy, ktoré obsahujú potrebné množstvo omega-3. Existujú tiež lieky, ktorých zloženie obsahuje omega-3 a ktoré sú schválené na použitie pri určitých ochoreniach srdca a ciev.
Ďalšie potenciálne účinky omega-3, vrátane protizápalových, sa skúmali pri najrozličnejších ochoreniach: reumatoidnej artritíde, zápalových ochoreniach čriev, depresii, syndróme deficitnej pozornosti a hyperaktivity, alergiách u detí, mukoviscidóze, vekovej makulárnej degenerácii, syndróme suchého oka, Alzheimerovej chorobe a iných stavoch. Avšak na rozdiel od všeobecne uznávaných účinkov a schválených indikácií na použitie sa účinky omega-3 v štúdiách týkajúcich sa týchto ochorení nevyznačovali konzistentnosťou a reprodukovateľnosťou.
Bolo vykonaných niekoľko systematických prehľadov randomizovaných kontrolovaných štúdií o účinkoch omega-3 pri jednotlivých zápalových ochoreniach. Autori jednej zo štúdií dospeli k záveru, že omega-3 mastné kyseliny môžu byť užitočné ako doplnok farmakoterapie na zmiernenie symptómov reumatoidnej artritídy, tento záver však vyžaduje potvrdenie v ďalších štúdiách [James M, 2010; Goldberg RJ, 2007]. Autori iného systematického prehľadu 19 štúdií o použití omega-3 pri zápalových ochoreniach čriev tvrdia, že dostupné údaje nepodporujú použitie omega-3 na indukciu alebo udržanie remisie týchto ochorení [Cabre E, 2012]. Sú potrebné ďalšie štúdie na presnejšie pochopenie možnej úlohy a miesta doplnkového použitia omega-3 pri zápalových ochoreniach. Vzhľadom na význam SPM pri riešení zápalu je však zrejmé, že účinná premena omega-3 na SPM je nevyhnutnou podmienkou na dosiahnutie prospešných doplnkových účinkov omega-3 v tejto situácii.
Ďalším prejavom zápalu súvisiacim s vekom je zápalové starnutie (inflammaging) – vekové zvýšenie hladiny mediátorov zápalu a rozvoj zápalového fenotypu. Predpokladá sa, že starnutie organizmu je spojené so zosilnením procesov nešpecifického zápalu a oslabením jeho riešenia. Mnohí autori nachádzajú súvislosti medzi inflammagingom, nedostatočnou hladinou SPM a niektorými chronickými ochoreniami spojenými s vekom: kardiovaskulárnymi ochoreniami spojenými s aterosklerózou; chronickým srdcovým zlyhaním, sarkopéniou, Alzheimerovou chorobou, obezitou, cukrovkou 2. typu, ochoreniami obličiek, patológiou kostí, zhoršením sluchu, dysbiózou a inými.
Dostupné údaje teda svedčia o tom, že nedostatočné potlačenie zápalu môže byť zapojené do patogenézy mnohých patologických stavov. Schopnosť SPM potláčať zápal bez ohrozenia obranyschopnosti organizmu z nich robí veľmi atraktívnych terapeutických kandidátov pri rôznych zápalových ochoreniach a stavoch, ale do veľkej miery závisí od ich efektívnej tvorby v organizme z omega-3. Ako tento potenciál SPM realizovať v praxi?
Ako zabezpečiť predvídateľnú premenu omega-3 na SPMv organizme pomocou... baktérií
Už sme sa presvedčili, že účinná premena omega-3 na SPM je nevyhnutnou podmienkou pre uplatnenie prospešných vlastností omega-3. Biosyntéza SPM závisí od mnohých faktorov a môže byť narušená v rôznych stavoch, čo čiastočne vysvetľuje nepresvedčivé a protichodné údaje o účinnosti použitia omega-3 v rade klinických situácií, o ktorých sme hovorili vyššie.
Na biosyntéze SPM sa podieľajú rôzne enzýmové systémy: lipoxygenáza (LOX), cyklooxygenáza typu 2 (COX-2) a cytochróm P450 monooxygenázy (CYP450). Táto biosyntéza je podrobne opísaná pre eukaryotické bunky, konkrétne pre granulocyty, monocyty a makrofágy. M2-makrofágy môžu exprimovať všetky enzýmy potrebné na biosyntézu SPM. 5-LOX sa nachádza v myeloidných bunkách, 12-LOX – v kožných a epitelových bunkách, 15-LOX – v dendritických a črevných gliových bunkách a izoformy COX-2 a CYP450 – v epitelových bunkách.
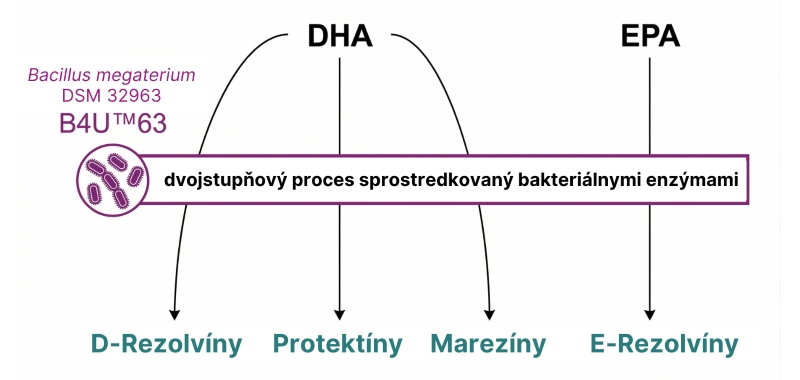
Existujú tiež údaje o oxidácii omega-3 enzýmami mikroorganizmov v GIT. Napríklad enzýmy CYP450s boli zistené u mikroorganizmov niekoľkých rodov typu Firmicutes, najmä rodu Bacillus. CYP102A1, tiež nazývaný CYP450BM3, je bifunkčný enzým zistený u baktérií druhu Bacillus megaterium, ktorý katalyzuje NADPH-dependentnú hydroxyláciu omega-3 mastných kyselín typu prostredníctvom postupných oxigenázových a reduktázových aktivít. Bolo preukázané, že purifikovaný CYP450BM3 získaný z konštrukcie expresného vektora generuje 18-HEPE z EPA v bezbuneckej reakcii.
S cieľom prekonať obmedzenia tradičných produktov obsahujúcich omega-3 a urobiť tento proces predvídateľnejším a nezávislým od rôznych vnútorných (genetika, mikrobióm, choroby) a vonkajších (špecifiká stravy, užívanie doplnkov stravy a liekov) faktorov, odborníci nemeckej spoločnosti Evonik Industries AG vyvinuli synbiotickú kompozíciu SynΩ3 (obsahujúcu probiotický mikroorganizmus a substrát pre neho), zabezpečujúcu nezávislú produkciu SPM priamo v organizme (in vivo). Bolo vykonané skúmanie 48 rôznych kmeňov Bacillus megaterium, ktoré ako živný substrát dostávali lysínovú soľ Omega-3 s vysokou biologickou dostupnosťou a v dôsledku toho produkovali široké spektrum SPM a ich prekurzorov. Okrem toho bola vykonaná analýza metabolitov baktérií a hodnotenie ich genómov. 5 [Speckman B, 2022] (pozri obr. 3).